發布時間:2024-05-28 瀏覽量:0

CAR-T細胞療法是一種特殊的免疫療法,通過遺傳修飾患者自身的T細胞,給T細胞安裝一個瞄準鏡,經過修飾的CAR-T細胞體外增殖后再輸注回患者體內,形成一支殺傷性的細胞部隊,能夠特異性地攻擊腫瘤細胞。
雖然CAR - T細胞在治療B細胞惡性腫瘤中已顯示出成功的臨床應用,但嚴重不良事件的發生是CAR - T細胞治療的一個重要限制,其中最受關注的不良反應為細胞因子釋放綜合征(cytokine release syndrome,CRS)。CRS是指在免疫細胞和腫瘤細胞作用的過程中,大量釋放細胞因子,這些細胞因子又會引發進一步的連鎖反應。細胞因子釋放綜合征的輕度臨床表現為發熱、疲勞、頭痛、關節痛、肌痛,嚴重者以低血壓、高熱為特征,進一步加重可引起休克、血管滲漏、彌散性血管內凝血和多器官功能障礙綜合征,最終危及生命。
那么是什么導致的CRS呢?研究表明,CD4+ CAR -T和CD8+ CAR -T細胞的比例是CRS相關的一項重要指標,然而,目前尚不十分清楚CD4+ CAR T細胞和CD8+ CAR T細胞對于引起CRS產生的作用是否相同。近期,來自巴斯德研究所的Philippe Bousso團隊通過研究發現, CRS的發生是主要由CD4+ CAR-T細胞介導的,而且在腫瘤負荷越高的情況下,CD4+ CAR T細胞介導的CRS反應越嚴重。相關研究發表在Cell Reports Medicine上。

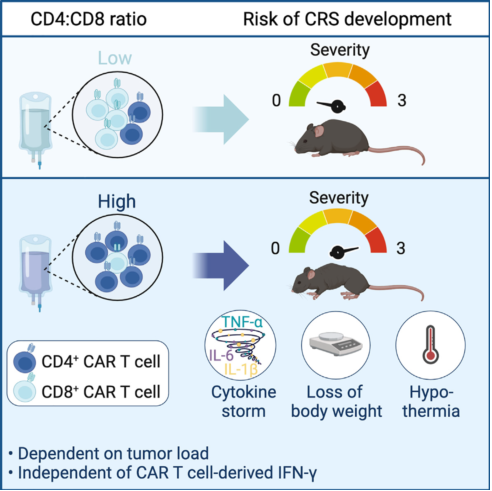
該團隊使用免疫健全的小鼠構建了Eμ-myc B細胞淋巴瘤小鼠模型。將小鼠分為純化的CD4+ CAR-T 治療組、純化的CD8+ CAR-T治療組和未治療組。結果顯示CD4+ CAR-T的輸注產生了明顯的毒性,治療第3天體溫急劇降低,體重下降,血清細胞因子和趨化因子普遍升高(圖3)。而且地塞米松和anti-IL-6的干預可以減輕體重的降低(圖4),這是臨床治療CRS的有效措施。而CD8+ CAR T的毒性表現則與對照組差別不大。說明CAR-T輸注后的毒性反應主要是由CD4+T細胞引起的,而不是CD8+T。
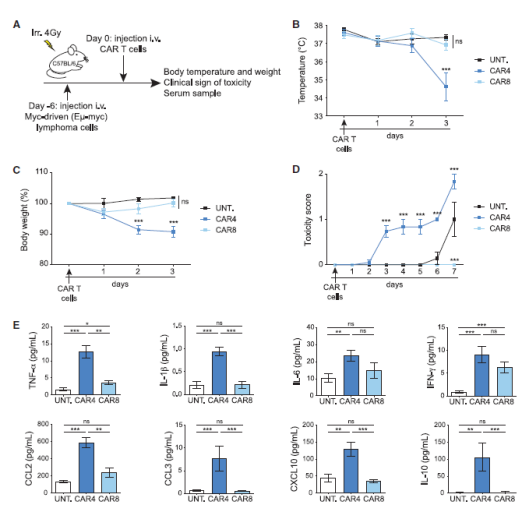
圖3. CD4+CAR-T和CD8+CAR-T輸注后,小鼠體征和血清細胞因子及趨化因子的變化
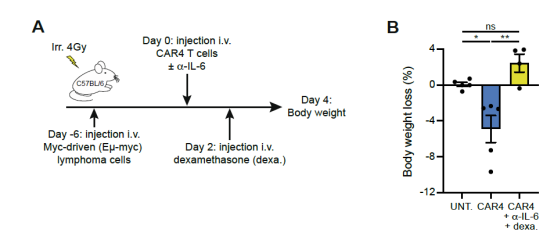
圖 4. 地塞米松和anti-IL-6的干預可以減輕CD4+CAR-T回輸后導致的體重降低。
接著,他們進行了CD4/CD8固定比例混合細胞的輸注。發現CD4/CD8比例為9:1時輸注也產生了與CD4+ CAR T相近的毒性,而CD4/CD8為1:1時則與陰性對照無差異(圖5)。說明CRS的發生不止局限于CD4+CAR-T,還發生在CD4+CAR-T占較高比例的混合CAR-T細胞中。
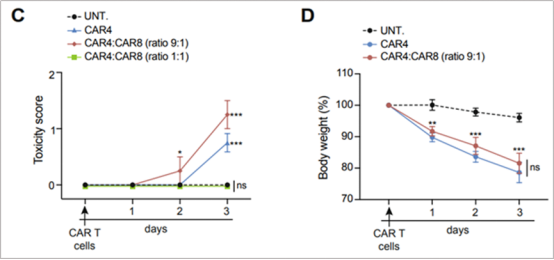
圖 5. 輸注混合CAR-T細胞CD4/CD8比例為9:1時產生更高的毒性。
為了驗證CAR-T細胞 與CRS等級的相關性,作者分析了76名接受CD19CAR-T治療的DLBCL患者血液中總CD3+CAR-T、CD4+ CAR T和CD8+ CAR T的細胞絕對數量。與未發生CRS的患者相比,發生1~3級CRS的患者,在回輸后第7天的峰值前后,其外周血中total CD3+ CAR T、CD4+ CAR T和CD8+ CAR T細胞的絕對數都更高。但CD4+ CAR -T細胞的增加更為明顯(圖6)。經歷CRS(1級、2級或3級)的患者比沒有經歷CRS(0級)的患者血液中CD4+ CAR - T細胞平均多3.43倍,而CD8+ CAR - T細胞平均多1.73倍。總之,這些臨床觀察結果與CD4+ CAR - T細胞在CRS誘導中起主要作用的觀點一致。
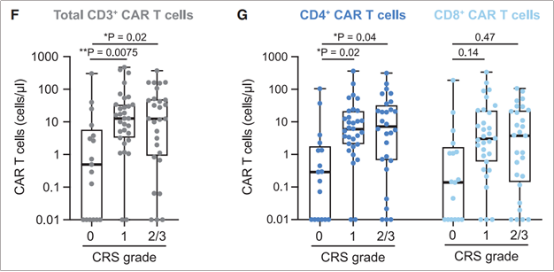
圖6. 患者CAR-T回輸后第7天的峰值前后,外周血中total CD3+ CAR T、CD4+ CAR T和CD8+ CAR T細胞數。
另外,作者還發現在與未經治療的小鼠相比,在高腫瘤負荷的情況下進行CD4+CAR-T細胞治療更容易引發CRS,包括體溫下降、體重減輕、疾病評分高和過早死亡(圖7) ,低腫瘤負荷的CAR4 T細胞治療沒有引發可檢測到的毒性。這也暗示CD4+CAR-T細胞占優勢加上高腫瘤負荷更容易導致CRS的發生。
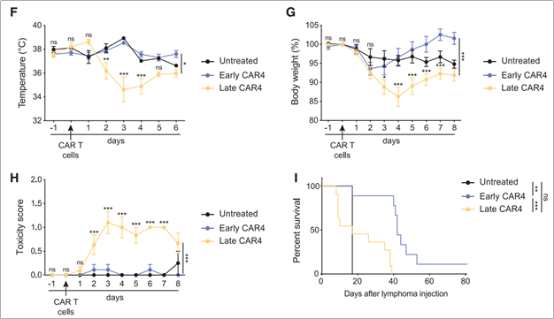
圖7. 在高腫瘤負荷的情況下進行CD4+CAR-T細胞治療更容易引發CRS
因此,針對患者的腫瘤負荷調整CD4:CD8 CAR - T細胞比例,為患者提供更加個性化的治療方案,可能更有助于減輕CAR - T細胞相關的毒性。
【注】文章內容旨在科普細胞知識,進行學術交流分享,了解行業前沿發展動態,不構成任何應用建議。


