發(fā)布時(shí)間:2023-08-07 瀏覽量:0
神經(jīng)退行性疾病是中樞神經(jīng)系統(tǒng)(CNS)的致命疾病,其特征是神經(jīng)系統(tǒng)內(nèi)特定蛋白質(zhì)的積累,伴隨神經(jīng)元的逐漸丟失。
但目前為止,其致病機(jī)制不完全清晰,神經(jīng)元變性的不確定原因?qū)е轮委熤袠猩窠?jīng)系統(tǒng)疾病缺乏有效的治療手段。其治療現(xiàn)狀面臨困境,即便是以改善患者生活質(zhì)量,延長(zhǎng)患者生命為目的的治療仍然具有挑戰(zhàn)性。
干細(xì)胞能在體外可分化為上皮細(xì)胞和來自神經(jīng)外胚層的譜系,修復(fù)損傷或病變的組織,因此被認(rèn)為是治療神經(jīng)退行性疾病的一種潛在的創(chuàng)新性治療策略。相比MSC的轉(zhuǎn)分化能力,其旁分泌作用,即通過細(xì)胞外囊泡(ev)的釋放來改變組織微環(huán)境的能力可能對(duì)組織修復(fù)的貢獻(xiàn)更為重要。
MSC治療的“生力軍”——MSC-Ev
細(xì)胞外囊泡(EV)是各種細(xì)胞釋放的膜性小泡,它包裹著干細(xì)胞生產(chǎn)的多種蛋白質(zhì)、RNA、酶類物質(zhì),與受損組織進(jìn)行信息交換或輸出,達(dá)到改善組織微環(huán)境,修復(fù)損傷細(xì)胞功能的作用。我們都知道,組成人體的器官或組織的基本單位就是細(xì)胞,所以,EV的治療具有從根本上延緩組織功能退化或喪失,起到直接修復(fù)組織功能的作用。相比單純的補(bǔ)充劑或抗炎類藥物,這也是我們關(guān)注或者更加看重干細(xì)胞或其衍生物治療效果的一個(gè)重要原因。
MSCs釋放大量具有高治療能力的Ev,這些Ev裝載了繁復(fù)的“活性藥物”——神經(jīng)營(yíng)養(yǎng)因子(NTFs)、免疫調(diào)節(jié)和抗炎分子,參與神經(jīng)發(fā)生和神經(jīng)保護(hù)的過程,促進(jìn)神經(jīng)功能恢復(fù)。例如,轉(zhuǎn)化生長(zhǎng)因子-β(TGF-β)、白細(xì)胞介素-10(IL-10),以及參與神經(jīng)發(fā)育和突觸發(fā)生的蛋白,如巢蛋白、生長(zhǎng)相關(guān)蛋白43(GAP-43)和突觸素等。大量的神經(jīng)退行性疾病的神經(jīng)病理學(xué)特征是細(xì)胞內(nèi)或細(xì)胞外蛋白原纖維的聚集,導(dǎo)致進(jìn)行性腦退行性變。
MSC-Ev中的酶類物質(zhì),在清除異常蛋白積累和抑制氧化應(yīng)激方面也起到重要作用。眾所周知,阿爾茨海默病(AD)的典型特征是淀粉樣蛋白(Aβ)的積累以及神經(jīng)原纖維纏結(jié)、突觸和神經(jīng)元的丟失,導(dǎo)致認(rèn)知功能的逐漸下降。而Ev中存在高水平的Aβ 降解酶被認(rèn)為是調(diào)節(jié)大腦中Aβ 積累水平的有效策略[1]。MSC-Ev中的抗氧化酶,如過氧化氫酶,可以保護(hù)海馬神經(jīng)元免受氧化應(yīng)激和突觸損傷[2]。此外,Ev中含有大量的效力miRNA,通過調(diào)節(jié)神經(jīng)發(fā)生和刺激軸突生長(zhǎng)來促進(jìn)中樞神經(jīng)系統(tǒng)恢復(fù)[3]。
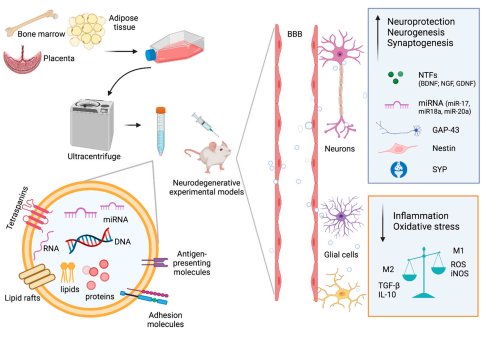
圖1 來自間充質(zhì)干細(xì)胞的細(xì)胞外囊泡
作為神經(jīng)退行性疾病的創(chuàng)新療法[4]。
MSC-Ev 的治療前景
MSC-Ev在一些中樞神經(jīng)系統(tǒng)疾病,如阿爾茨海默病(AD)、帕金森病(PD)和肌萎縮性側(cè)索硬化癥(ALS)等中都表現(xiàn)出良好的治療潛力。在AD患者中, Aβ的低聚化、過度神經(jīng)興奮、神經(jīng)炎癥等都會(huì)導(dǎo)致NO的產(chǎn)生,繼而發(fā)生S-亞硝基化。MSC-Ev在減少氧化損傷和亞硝化損傷方面具有治療作用。在PD、酒精相關(guān)的腦損傷、腦缺血性損傷等模型中,MSC-Ev對(duì)包括神經(jīng)元和膠質(zhì)細(xì)胞在內(nèi)的多種細(xì)胞類型有影響,可以改善線粒體功能障礙引起的氧化應(yīng)激損傷,對(duì)抗神經(jīng)退行性變。在抗炎功效中,MSC-Ev的治療,可以增加Foxp3+CD25+調(diào)節(jié)性T細(xì)胞的比例,在AD小鼠模型中誘導(dǎo)了很強(qiáng)的抗炎作用,改善了M2極化的巨噬細(xì)胞的數(shù)量。
人臍帶來源的間充質(zhì)干細(xì)胞中分離出的Ev顯著增強(qiáng)了Aβ 降解酶的表達(dá),減少了AD小鼠的Aβ 沉積,減少了神經(jīng)炎癥,提高了小鼠認(rèn)知能力[5]。XFAD AD小鼠存在血腦屏障的滲漏,而Ev被證明能夠啟動(dòng)和修復(fù)血腦屏障的滲漏,逆轉(zhuǎn)由AD誘導(dǎo)的血腦屏障的缺陷。不同來源的MSC-Ev能夠促進(jìn)多巴胺能神經(jīng)元對(duì)氧化應(yīng)激的神經(jīng)保護(hù),減少黑質(zhì)多巴胺能神經(jīng)元的丟失、凋亡,并上調(diào)紋狀體中的多巴胺水平。在PD大鼠模型中,MSC-Ev治療可以改善小鼠運(yùn)動(dòng)能力。運(yùn)動(dòng)神經(jīng)元(MNs)是肌萎縮性側(cè)索硬化癥(ALS)的主要靶點(diǎn),因?yàn)樯稀⑾翸Ns的選擇性功能障礙和損傷導(dǎo)致進(jìn)行性癱瘓和死亡。MSC-EV已經(jīng)證明能夠調(diào)節(jié)病理SOD1蛋白的聚集,恢復(fù)G93A突變的ALS小鼠和MN培養(yǎng)的神經(jīng)元線粒體蛋白水平。總的來講,MSC-Ev可以減少氧化應(yīng)激和亞硝化損傷,作為炎癥成分“調(diào)節(jié)劑”和異常蛋白積累“消除劑”,對(duì)抗神經(jīng)退行性變。
MSC-Ev 的治療策略
1、如何精準(zhǔn)傳遞至中樞神經(jīng)病變區(qū)域
中樞神經(jīng)系統(tǒng)疾病治療的兩個(gè)關(guān)鍵問題,首當(dāng)其沖是如何通過血腦屏障(BBB)的通道有效使治療藥物傳遞至中樞神經(jīng)系統(tǒng)病變區(qū)域。血腦屏障是一種選擇性滲透的膜,調(diào)節(jié)外周血管循環(huán)和中樞神經(jīng)系統(tǒng)之間物質(zhì)的通道,從而保護(hù)中樞神經(jīng)系統(tǒng)免受有害物質(zhì)或過度免疫反應(yīng)的影響,而能夠突破BBB是Ev的重要優(yōu)勢(shì)。由于其體積小,MSC-Ev能夠在輸注后有效地遷移到目標(biāo)器官,而不會(huì)被困在肺毛細(xì)血管中,穿過血腦屏障,到達(dá)大腦中的損傷區(qū)域。
另一方面,能夠?qū)崿F(xiàn)無創(chuàng)的治療新形勢(shì),也是Ev的優(yōu)勢(shì),如通過鼻腔給藥,跳過胃腸道和肝臟代謝,增加吸收,減少劑量,以達(dá)到增效的治療效果。利用簡(jiǎn)單有效地設(shè)備,如滴劑,氣霧劑,噴霧劑等,MSC-Ev可通過嗅球直接進(jìn)入大腦,進(jìn)入腦脊液或通過三叉神經(jīng)途徑從鼻上皮到體循環(huán)。與其他侵入式給藥途徑相比,鼻內(nèi)給藥在侵襲性和患者依從性方面占有優(yōu)勢(shì)。
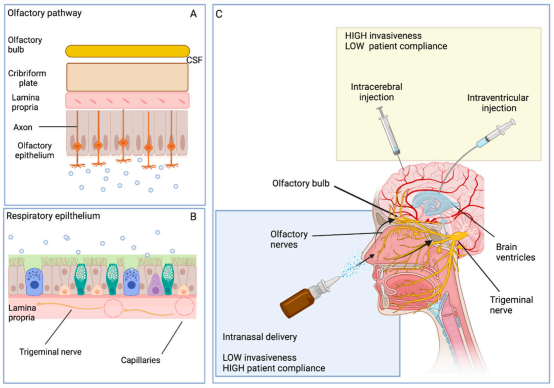
圖2. msc-ev的鼻內(nèi)傳遞[4]。
2、如何提高藥物保留時(shí)間
給藥濃度、劑量和給藥量是影響鼻腔藥物進(jìn)入大腦的重要因素。粘液纖毛清除是鼻內(nèi)給藥動(dòng)力學(xué)的一個(gè)限制因素。特別是,細(xì)胞色素P450、肽酶和蛋白酶等降解酶的存在可以對(duì)藥物和細(xì)胞成分的代謝產(chǎn)生影響。之所以說MSC-Ev大有可為,不僅僅是其獨(dú)特的生物學(xué)優(yōu)勢(shì),另外,其體外的“可操作性”——?jiǎng)?chuàng)新結(jié)合和工程化改造,讓人們有更多的思路或者手段探討提高M(jìn)SC-Ev治療效果的策略。
比如在生物技術(shù)領(lǐng)域已經(jīng)通過添加吸收增強(qiáng)劑、粘附聚合物、原位膠凝劑、酶抑制劑和生物活性支架來延長(zhǎng)藥物在鼻腔內(nèi)的停留時(shí)間,從而獲得更高的生物利用度。工程化改造策略包括提高突破BBB的MSC-Ev的數(shù)量和濃度,提高特別靶向小膠質(zhì)細(xì)胞和少突膠質(zhì)細(xì)的能力,通過納米工程提高M(jìn)SC-Ev的生物利用度,提高EV在體循環(huán)中的穩(wěn)定性等。
【參考文獻(xiàn)】
[1] Katsuda, T., et al., Human adipose tissue-derived mesenchymal stem cells secrete functional neprilysin-bound exosomes. Sci Rep, 2013. 3: p. 1197.
[2] de Godoy, M.A., et al., Mesenchymal stem cells and cell-derived extracellular vesicles protect hippocampal neurons from oxidative stress and synapse damage induced by amyloid-β oligomers. J Biol Chem, 2018. 293(6): p. 1957-1975.
[3] Vila?a-Faria, H., A.J. Salgado, and F.G. Teixeira, Mesenchymal Stem Cells-derived Exosomes: A New Possible Therapeutic Strategy for Parkinson's Disease? Cells, 2019. 8(2).
[4]Turano, E., et al., Extracellular Vesicles from Mesenchymal Stem Cells: Towards Novel Therapeutic Strategies for Neurodegenerative Diseases. Int J Mol Sci, 2023. 24(3).
[5]Ding, M., et al., Exosomes Isolated From Human Umbilical Cord Mesenchymal Stem Cells Alleviate Neuroinflammation and Reduce Amyloid-Beta Deposition by Modulating Microglial Activation in Alzheimer's Disease. Neurochem Res, 2018. 43(11): p. 2165-2177.



