發布時間:2023-08-03 瀏覽量:0
細胞外囊泡 (EVs)是由細胞釋放的膜狀天然納米顆粒,作為天然的納米顆粒,EV固有地受益于免疫耐受性、循環系統的穩定性以及穿越生物屏障到達大腦等遠處器官的能力。
為了準確評估EVs的治療潛力,體內應用實驗是必不可少的。準確可靠的給藥策略對正確評估EV的治療效果(最低藥效學劑量)、藥效動力學(PD)和藥代動力學(PK)至關重要。
Part 1 EVs應用劑量大有考究
不同的實驗動物(大鼠、小鼠、豬)、給藥途徑(系統性/局部)、研究領域(心血管、神經、炎癥、癌癥)等,臨床前以及臨床上所用的EVs劑量大有考究。
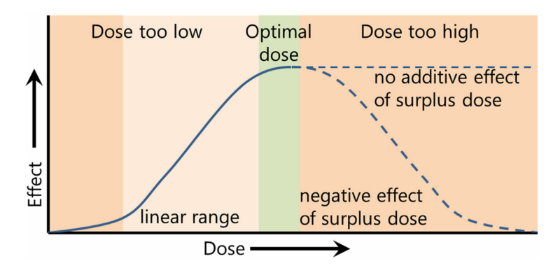
△圖1.EVs量效關系圖
Part 2 EVs劑量的影響因素
1.計量方法(蛋白量/顆粒數)與劑量
大多數研究以蛋白量來量化EVs在體內的應用劑量,部分研究以RPS或NTA計算EVs的顆粒數,以顆粒數量化EVs在體內的應用劑量。但無論哪種計量方法,EVs有效劑量的范圍、治療頻次均存在很大的差異。
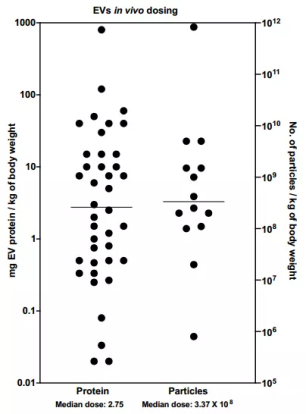
△圖2.計量方法(蛋白量/顆粒數)與EVs劑量
2.給藥方式與劑量
體內實驗的給藥方式分為系統給藥和局部給藥,通過統計分析動物實驗所用EVs的給藥方式發現,系統性給藥途徑的應用較多,如靜脈注射。
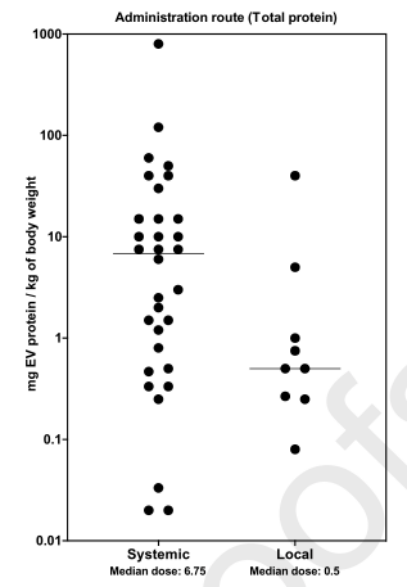
△圖3.給藥方式與EVs劑量
3.實驗動物與劑量
研究中EVs劑量的變化是否主要是由于動物物種的差異?
由于高等動物的代謝率和體表面積重量比較低,大型動物往往需要較低的劑量才能觀察到類似的治療效果。大型動物的中位治療劑量低于小型動物。
因臨床前使用的動物種類不同,缺乏對體內劑量反應動力學進行全面評估的研究,目前仍無法解決EVs給藥不一致的問題。
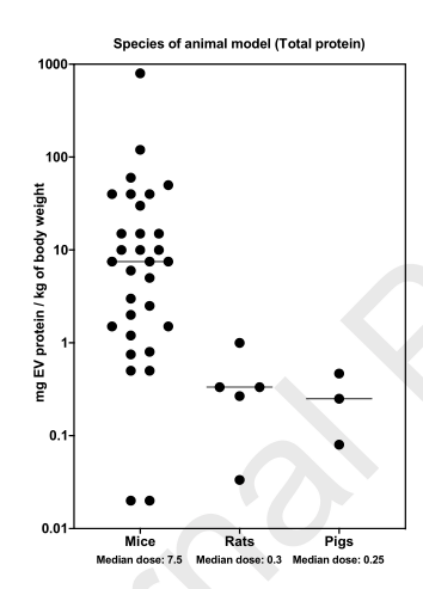
△圖4.實驗動物與EVs劑量
4.制備方式與劑量
直接分離方法(如沉淀或超濾),根據大小或密度使用EVs純化方法(超離、尺寸排阻等),用于EVs純化的技術會影響最終制備中外泌體的總蛋白質數量。有趣的是,使用直接分離方法(如沉淀或超濾)的研究中的中位治療劑量比使用基于大小或密度的EVs純化方法的研究低約10倍。
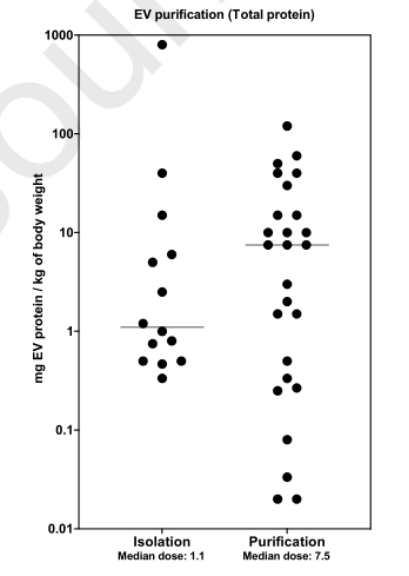
△圖5.制備方式與EVs劑量(蛋白計量)
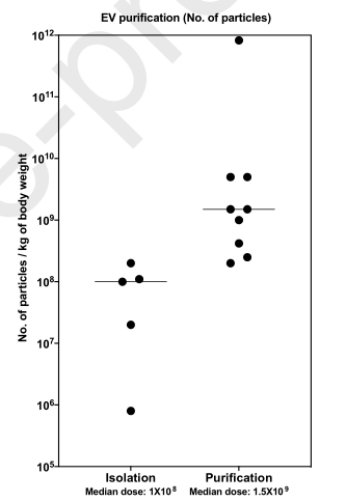
△圖6.制備方式與EVs劑量(顆粒數計量)
5.適應癥與EVs劑量
不同適應癥動物實驗所用的EVs劑量也存在很大差異,目前研究較多的是心血管疾病、神經系統疾病、炎癥性疾病等。大多數EVs藥代動力學研究都是在野生型(WT)動物模型中進行的。
由于EVs具有靶向目標病變器官的能力,EVs在患病動物中的分布也可能存在很大的差異。
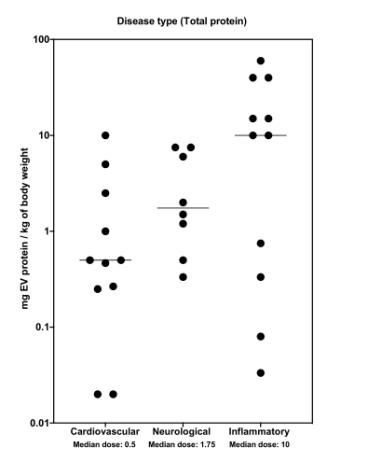
△圖7.適應癥與EVs劑量
Part 3 文末小結
目前外泌體臨床前研究的實驗動物以小鼠為主,給藥方式多為尾靜脈注射。大多數已發表的關于間充質細胞及其細胞外囊泡的臨床試驗均為靜脈給藥方式。在這些研究中,雖然治療的安全性已經得到肯定,但它們的治療效果并不顯著,這或許在于給藥劑量的差異。不同研究中使用的外泌體劑量不盡相同,因此以上內容僅供參考,具體用量建議正式實驗前,可通過設置不同劑量梯度的預實驗來摸索合適的外泌體用量。
盡管外泌體在動物實驗及臨床應用上取得不錯的進展,但外泌體的純化方法、表征、定量方式等缺乏統一的標準,不同研究之間差異較大,因此需要建立統一的標準操作流程和檢測方法,保證批次間的可靠性,提高應用之間的可重復性。
山東省齊魯細胞治療工程技術有限公司以標準化、良好表征、經過中檢院質量復核的臍帶間充質干細胞作為外泌體制備的種子細胞,建立了標準化可量產的外泌體純化平臺以及完善的檢測體系。


△圖8. 外泌體制備與檢測鑒定平臺
參考資料
[1]Gupta D, Zickler AM, El Andaloussi S. Dosing extracellular vesicles. Adv Drug Deliv Rev. 2021 Nov;178:113961. doi: 10.1016/j.addr.2021.113961. Epub 2021 Sep 2. PMID: 34481030.



