發布時間:2024-06-20 瀏覽量:0

在接受靶向CD19的嵌合抗原受體(CAR)T細胞免疫治療的患者中,超過一半的患者沒有獲得持久的緩解, PD-1/PD-L1相關的CAR-T細胞功能障礙是可能的部分原因。
PD-1是一種膜受體蛋白,主要存在于免疫細胞表面,如T細胞和B細胞等。通過調節免疫系統對人體細胞的反應,以及通過抑制T細胞炎癥活動來調節免疫系統并促進自身耐受。PD-L1是PD-1的配體蛋白,是大小為40KDa的第一型跨膜蛋白。主要存在于免疫細胞和某些非免疫細胞表面。PD-1可與PD-L1結合,通過PD-1/PD-L1通路降低CD8+T淋巴細胞及 CD4+T淋巴細胞活性,并抑制二者增殖,進而抑制腫瘤局部微環境中T淋巴細胞發揮作用,對腫瘤的免疫殺傷功能降低,腫瘤易發生免疫逃逸。在對CD19CAR-T細胞免疫治療未能獲得持久應答的患者的預處理腫瘤活檢標本中觀察到PD-L1的高表達。[1]這些數據表明,中斷PD1/ PD-L1軸可能會提高CAR-T細胞治療的成功率。
利伯蒂·巴普蒂斯特學院的一項小型1期臨床試驗報告了CD19CAR-T細胞治療后LBCL進展的患者對抗PD1單克隆抗體治療的反應。[2]然而,CD19CAR-T細胞聯合免疫檢查點封鎖(ICB)免疫治療的研究數據令人失望。[3]CD19CAR-T細胞聯合ICB治療失敗的原因尚不清楚。此外,這些研究并沒有能力解決聯合治療方案的差異。
有研究表明,PD-L1抑制劑優于PD-1抑制劑,因為嚴重不良事件(AEs)的風險較低,特別是免疫相關的AEs。[4]
2024年Alexandre V. Hirayama[5]等報告了一項1期臨床試驗( NCT02706405) 的 數 據 ,該成人大B細胞淋巴瘤(LBCL)患者使用自體CD19CAR-T細 胞聯合劑量不斷增加的抗PD-L1單克隆抗體durvalu單 抗治療。
患者分成2組,如圖1所示,1組患者最初在CD19CAR-T后21天內 開始接受第一劑量的durvalu單抗。在安全性分析后,隨后的患者在CD19CAR-T后7天開始接受durvalu單抗治療。2組患者在CD19CAR-T給藥前 1天首次給予durvalu單抗。第1組和第2組首次輸注durvalu單抗的劑量水平列于表1。對于兩組,在注射CD19CAR-T輸注后,以確定的最高安全劑量給予至多10個周期,直到不可接受的毒性或疾病進展 。
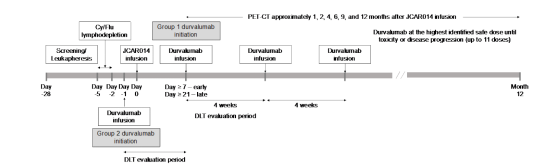
圖1:治療方案。Cy,環磷酰胺;DLT,劑量限制毒性;Flu,氟達拉濱。
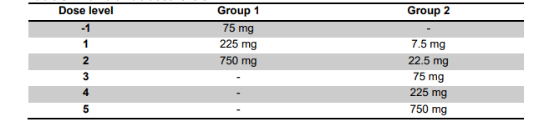
表1 durvalu單抗的劑量水平
我們對ICB與CD19CAR-T的聯合使用的安全性進行了評估。結果顯示,≥1級和≥3CRS和神經毒性的發生率與之前的經驗一致,2個治療組之間相似(表2)。然而,與組1相比,組2患者在CAR-t細胞輸注后CRS發病較晚(中位數6vs4天;P =.05),CRS持續時間較短(中位數3 vs 8天;P =.08;表2 )。
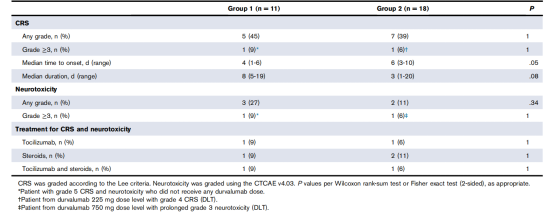
表2 CRS反應和神經毒性
LBCL患者接受相同的Cy/Flu淋巴清除術和相同的CAR-T細胞回輸劑量(2×10^6/kg)。與單獨使用CAR-T細胞治療的患者相比,CAR-T細胞聯合durvalu單抗治療的患者ORR(P = .08)和CR率(P = .09)有較低的趨勢(表3)。盡管腫瘤負荷較低,但第2組患者(CAR-T細胞前首次使用durvalumab)的CR率及ORR率均低于第1組治療患者(CAR-T細胞后首次使用durvalu單抗;P=。16)。1組患者(CAR-T細胞后首次使用durvalumab)與單獨接受CD19CAR-T 組患者的ORR和CR率無顯著差異。這些數據表明,在CAR-T細胞回輸之前應用durvalumab單抗患者整體療效較差。
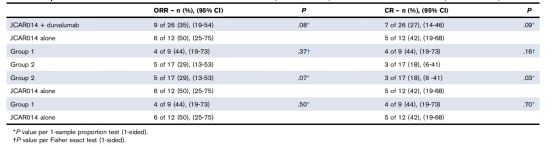
表3 ICB與CD19CAR-T的聯合使用的有效率
長期隨訪結果顯示,接受CD19CAR-T和單抗藥物的患者DOR優于單獨接受CD19CAR-T(1年DOR估計,67%;95% CI,42-100vsDOR,20%;95% CI,3-100;圖2)。我們認為,盡管有一部分患者最初的反應較差,但隨后每月注射durvalumab可能有助于改善CD19CAR-T后的DOR。
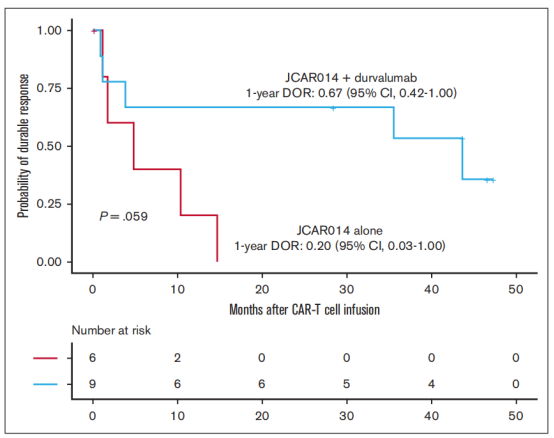
CD19CAR-T + durvalumab或者CD19CAR-T 單獨治療后患者DOR。持續緩解時間(DOR)
總之,PD-L1阻斷的應用時間是影響成人LBCL接受CD19CAR-T細胞免疫治療后預后的一個關鍵變量。對于PD-L1單抗和CD19CAR-T聯合應用的探索是目前臨床研究的熱點之一。
【注】文章內容旨在科普細胞知識,進行學術交流分享,了解行業前沿發展動態,不構成任何應用建議。


