發布時間:2023-07-19 瀏覽量:0
近年來,乳腺癌已成為對婦女健康危害最嚴重的腫瘤之一,每年大約有數十萬人死于乳腺癌。
根據2020年數據顯示,目前在全球范圍內,乳腺癌新增人數達226萬,已超過肺癌,成為全球發病人數最多的腫瘤。盡管早篩技術和診療方式的進步提高了乳腺癌患者的生存率和生活質量,但是由于耐藥性的出現,晚期乳腺癌患者的死亡率仍舊很高。
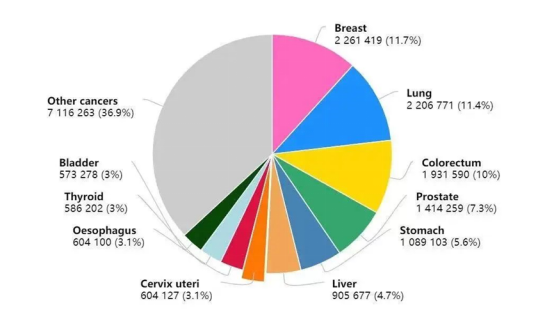
△2020年癌癥新發病例數前十的癌癥類型
2013 年腫瘤免疫治療被評為世界十大科技突破之首,繼2017 年美國FDA批準兩款CD19 CAR-T細胞藥品上市,后續又有6款CAR-T上市用于治療血液瘤,腫瘤細胞免疫治療成為傳統治療手段之外最具價值和發展潛力的治療手段。
面對來勢洶洶的乳腺癌,醫學專家們也在積極開發新的治療方式,其中CAR-T療法就是重要的治療方式之一。
CAR-T細胞靶點分為兩類:腫瘤特異性抗原(TSA)和腫瘤相關性抗原(TAA)。由于腫瘤特異性抗原較為缺少,目前報道的實體腫瘤CAR-T細胞臨床試驗大多都圍繞著腫瘤相關性抗原構建,其中包括間皮素(MSLN)、神經節苷脂 2(GD2)、人類表皮生長因子受體2(Her-2)、癌胚抗原(CEA)、前列腺特異性膜抗原(PSMA)等。
隨著不同靶點 CAR-T細胞臨床試驗的進展,實體瘤中的腫瘤靶點選擇被認為有更多重要的作用。乳腺癌也是一種異質性很強的疾病,對于包括TNBC在內的沒有ERBB2和HR表達的組織,尋找有效靶點,是亟待解決的難題。
目前已有一些臨床前實驗顯示CAR-T對乳腺癌治療具有積極的療效,也有多項CAR-T 治療乳腺癌的臨床試驗正在各自開展中。
本文對目前用于治療乳腺癌的潛在靶點進行盤點歸納,希望能為乳腺癌的治療提供一些思路。
臨床試驗中CAR-T治療乳腺癌的潛在靶點總結如下表:
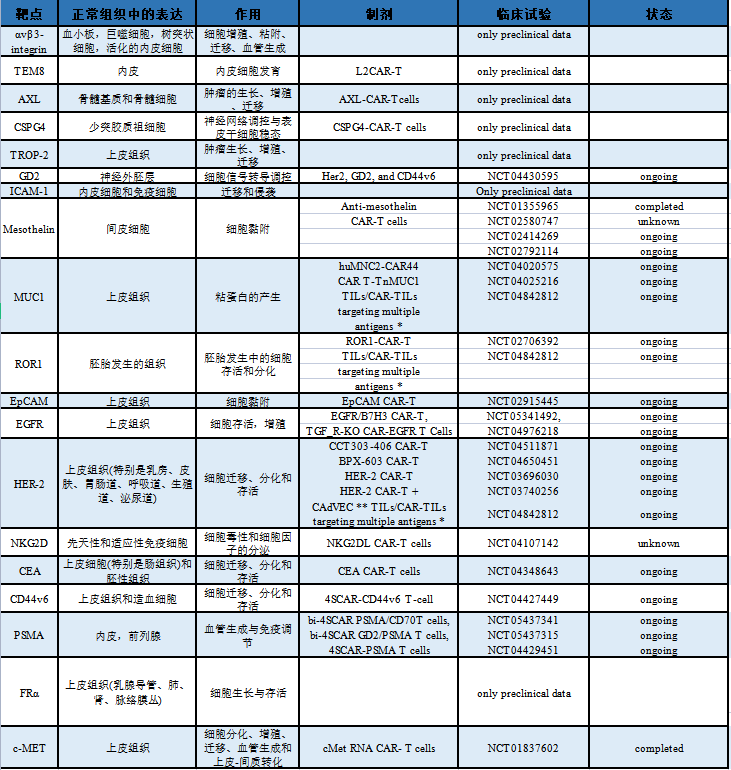
【釋義】
*靶向HER2、Mesothelin、PSCA、MUC1、Lewis-Y、GPC3、AXL、EGFR、Claudin18.2/6、ROR1、GD1或B7-H3的TILs和CAR-TILs。
**CAdVEC是一種溶瘤腺病毒,旨在幫助免疫系統,包括HER2特異性CAR-T細胞,對腫瘤作出反應。
表格引自 Giuseppe Schepisi,etal.,2023.
乳腺癌根據分子表型臨床上分為三種亞型:Luminal型乳腺癌,HER-2陽性乳腺癌和三陰型乳腺癌。
CAR-T與HER-2陽性乳腺癌
其中HER-2陽性的患者占到了大約20%-30%。該亞型對內分泌治療不敏感,預后差,在乳腺癌中排名第二。HER-2水平升高與乳腺癌患者的生存率降低有關,因此靶向HER2 的CAR-T 療法在乳腺癌的CAR-T 治療中起著非常重要的作用。
2014年,Sun等以HER-2為靶點制備CAR-T細胞,體外殺傷HER-2+乳腺癌細胞(SKBR3、MCF-7和T47D細胞系),抑制皮下移植小鼠SKBR3細胞的腫瘤生長。在HER-2轉基因小鼠中觀察到對乳腺癌的抑制作用。HER-2 CAR-T細胞聚集在原發病灶,多次輸注后可抑制復發和轉移。
Szoor等人發現靶向HER-2 CAR-T細胞穿透腫瘤細胞球引起細胞毒性,抑制含有曲妥珠單抗耐藥乳腺癌細胞(MDA-HER-2)的小鼠的生長。
然而目前靶向HER-2 的CAR-T 治療臨床試驗大多是針對膠質母細胞瘤,針對乳腺癌的臨床試驗結果尚未公開。其中一項臨床研究(NCT04650451)評估HER-2特異性雙開關CAR-T細胞BPX-603 BPX-603與rimiducid一起應用于先前治療過的HER-2擴增/過表達的局部晚期或轉移性實體瘤患者,評估CAR-T的有效性和安全性,預計研究完成日期為2025年1月2日。
另一項研究是在晚期HER-2陽性實體瘤患者中進行的溶瘤腺病毒聯合HER-2CAR-T細胞的治療,試驗已經招募了45名HER-2陽性腫瘤患者,預計研究完成日期為2038年12月30日(NCT03740256)。
這些臨床試驗可能會為乳腺癌腦轉移患者帶來康復的解決方案。
CAR-T與三陰乳腺癌
三陰乳腺癌作為其中一類獨立亞型,是指雌激素受體(ER)、孕激素受體(PR)、人表皮生長因子受體2(HER2)三者均為陰性表達的乳腺癌,占全部乳腺癌的15~20%。它具有高侵襲性、易轉移復發、預后差等特點,因此其患者總生存期的中位數為9~13 個月,遠遠低于非三陰乳腺癌患者。
在所有乳腺癌亞型中,EGFR在TNBC中的表達高于其他亞型(66.7% vs 9.1%)。林霞等發現EGFR CAR-T細胞在體外和體內對TNBC細胞的生長都有有效的特異性抑制作用。CAR-T治療2個月后,他們觀察到異種移植小鼠模型(TNBC腫瘤發生)的生存期延長(p < 0.001)并抑制肺轉移。針對EGFR的臨床I期研究NCT05341492納入了30例患者(包括EGFR/ B7-H3陽性晚期肺癌和EGFR/ B7-H3陽性晚期TNBC),每例患者接受2 × 106個CAR-T細胞/kg。研究結果可為應用EGFR特異性CAR-T治療乳腺癌提供參考。

乳腺癌病例(226例TNBC和88例非TNBC)的免疫組化染色顯示TNBC中間皮素(MSLN)表達較高(分別為36%和16%)。由于MSLN在正常組織中幾乎不表達,它可能是TNBC理想的CAR-T細胞治療靶點。體外結果顯示,靶向MSLN的CAR-T細胞對乳腺癌細胞具有毒性。MSLN特異性CAR-T細胞的I期臨床試驗顯示,沒有細胞因子釋放綜合征、神經毒性或對正常組織的毒性。另外三項使用靶向CAR-T細胞治療乳腺癌的臨床研究正在進行中:NCT02792114(轉移性HER-2陰性乳腺癌)、NCT02414269(胸膜轉移性乳腺癌)和NCT02580747 (TNBC)。然而,這些臨床試驗的結果大多尚未公開,需要更多關于MSLN-CAR-T的劑量和療效的臨床試驗來證實其治療乳腺癌的有效性。
ROR1 在胚胎中的表達量較高,但在成體細胞中的表達量有限,乳腺癌中ROR1 的高表達與預后不良有關,因而被當作CAR-T 靶點研究。在2018 年底的第41 屆圣安東尼奧乳腺癌研討會SABCS 上公布的一項研究(I 期試驗的初步結果),之前接受過多種療法的三陰乳腺癌患者在ROR1CAR-T 細胞療法后病情穩定(1 例15 周,1 例19 周),一名患者在第一次輸注后病情穩定,第二次出現持續14 周的部分應答。

但是也出現了一些問題:CAR-T細胞在輸注后第14 天出現了“衰竭”的表型。TGF-β 可以抑制細胞因子的產生以及CAR-T 細胞的殺傷、增殖能力,ROR1 CAR-T 和TGF-β 受體I 激酶抑制劑SD-208 的聯用可以中和TGF-β 的免疫抑制作用,改善CAR-T 的效果。
c-Met 是在乳腺癌等多種實體瘤中表達的細胞表面蛋白酪氨酸激酶,研究發現c-Met在50%的乳腺癌中表達。單價抗c-Met 抗體Onartuzumab 已在臨床試驗中對多種晚期實體癌患者進行了療效測試。有研究團隊利用mRNA 制備CAR-T技術開展了該靶點在三陰乳腺癌中的研究(NCT01837602),該結果表明c-Met CAR-T可以輸送入實體腫瘤部位,耐受性良好并在腫瘤內引起炎癥反應。這一結果可為實體瘤的治療提供參考。
總而言之,近年來針對乳腺癌的CAR-T細胞療法臨床試驗盡管注冊較多,但是少有結果發表,需要更多的研究來驗證和比較乳腺癌不同靶標的有效性。盡管在實體瘤上的臨床應用會面臨一些極大的挑戰,但依舊期待CAR-T療法在不遠的將來會在實體瘤中提高療效。
【參考文獻】
1. Giuseppe Schepisi, Caterina Gianni, Michela Palleschi, etal. The New Frontier of Immunotherapy: Chimeric Antigen Receptor T (CAR-T) Cell and Macrophage (CAR-M) Therapy against Breast Cancer [J]. Cancers, 2023,15(5),10.3390/cancers15051597.
2. Li Yin, Gui-Lai Chen , Zhuo Xiang, etal. Current progress in chimeric antigen receptor-modified T cells for the treatment of metastatic breast cancer [J]. Biomed Pharmacother, 2023 Jun;162:114648. doi: 10.1016/j.biopha.2023.114648.
3. Julia Tchou ,Yangbing Zhao, Bruce L Levine, etal. Safety and efficacy of intratumoral injections of chimeric antigen receptor (CAR) T cells in metastatic breast cancer[J]. Cancer Immunol Res. 2017,5(12): 1152–1161.


