發布時間:2025-12-30 瀏覽量:0
前言
INTRODUCTION
帕金森是一種神經退行性疾病,其特征是由于黑質中多巴胺能神經元的選擇性喪失而引起的運動障礙,又稱為“震顫麻痹”。其典型臨床表現為靜止性震顫、行動遲緩、肌強直姿勢步態障礙等。除了常見的運動癥狀外,帕金森病患者同時還會伴有便秘、嗅覺減退、焦慮抑郁、睡眠障礙、感覺異常等非運動癥狀。

帕金森病的手抖癥狀有以下4個特點:
● 靜止時明顯。
● 精神緊張時加重。
● 做隨意動作時減輕。
● 睡眠時消失。
動作遲緩是帕金森病的核心癥狀:
● 在做起床翻身、刷牙洗臉等日常活動時,動作變得遲緩。
● 缺乏面部表情,不眨眼、雙眼凝視,笑容緩慢出現和消失。
● 聲調變低,言語不清。
● 寫出的字小而彎曲,難以辨讀。
帕金森病目前治療主要以藥物治療為主,輔以康復鍛煉,必要時可以考慮手術治療,主要通過提高腦內紋狀體多巴胺水平來達到治療目的。但是傳統的治療方法無法逆轉神經變性,同時也無法增加多巴胺能神經細胞的數目。因此,從病因上尋求一種提高神經細胞數目的治療方式的突破具有重要意義。
國外一研究團隊發表于《Cells》的綜述,以帕金森為例系統闡述了MSC-Evs(包含間充質干細胞外泌體)在改善腦部健康,包括改善睡眠及保護神經等方面的作用機制和潛在應用價值。

帕金森病(PD)是一種進行性神經退行性疾病,其特征是大腦黑質致密部內產生多巴胺的神經元逐漸喪失。全球約有超過1000萬人患有帕金森病,這種第二大常見的神經退行性疾病正隨著人口老齡化而不斷增加。傳統的藥物治療雖能在早期緩解癥狀,卻難以阻止疾病進展,且長期使用會產生副作用。
近年來,科學家們將目光投向再生醫學領域,尤其是MSC-Evs在改善帕金森病等神經退行性疾病方面的潛力。
MSC-Evs是細胞分泌的細胞外囊泡(包含外泌體),攜帶蛋白質、RNA(特別是miRNA)和脂質等生物活性分子,作為細胞間通信的重要媒介。
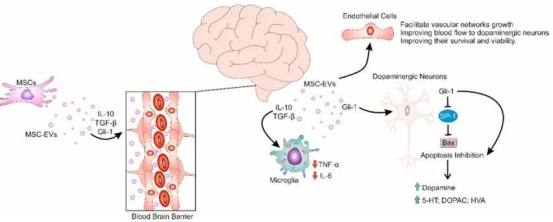
1. 可穿過血腦屏障,并將各種神經營養因子和免疫抑制因子遞送至受損多巴胺能神經元,增強其活力和功能。
2. 可減弱小膠質細胞驅動的炎癥反應,并預防炎癥誘導的多巴胺能神經元損傷。
3. 通過遞送IL-10和TGF-β,抑制炎性細胞因子的產生(TNF-α和IL-6),并增加多巴胺、5-羥色胺(5-HT)及其代謝產物的產生。
4. MSC-EVs來源的Gli-1通過抑制特異性蛋白1(SP-1)的激活,增強促凋亡Bax基因的表達,從而抑制多巴胺能神經元的凋亡。
5.通過激活腦內皮細胞中的SMAD 3和p38/MAPK信號通路,促進血管網絡的生長,其改善了向受損多巴胺能神經元的血流。
6.攜帶的多種具有神經保護和免疫調節能力的miRNA,可調節基因表達,防止細胞凋亡,并促進多巴胺能神經元的恢復力。
超過75%的帕金森病患者伴有嚴重的睡眠障礙,這已成為影響生活質量的主要因素之一。傳統安眠藥物雖然短期內可改善睡眠,但長期使用會導致依賴性、耐受性,甚至可能加重認知障礙。因此,尋找既能治療帕金森病核心癥狀又能改善睡眠的新方法成為當務之急。
研究發現,MSC-Evs可誘導腦和肌肉Arnt樣蛋白-1(BMAL 1)和周期晝夜節律調節因子2(PER 2)蛋白的合成增加,其是調節晝夜節律、代謝和受損神經元活力的生物鐘的組成部分。
另有動物實驗顯示,MSC-EVs治療的PD大鼠的總睡眠時間、慢波睡眠時間和快波睡眠時間延長,這表明MSC-EVs通過恢復晝夜節律相關基因表達來顯著改善PD大鼠的睡眠障礙。
間充質干細胞外泌體作為一類具有多重神經保護功能的納米載體,通過促進血管生成、調節神經炎癥、抑制細胞凋亡和氧化應激、增強自噬等多種機制,在腦部健康的臨床干預中展現出巨大潛力。

針對帕金森,現有研究中所用到的使用方也較為豐富,如齊魯細胞公司與上海瑞金醫院聯合開展的“臍帶間充質基質細胞來源外泌體治療帕金森病的安全性和有效性臨床研究”項目中所用到的鼻噴的形式,這種遞送方式,相較于傳統的口服或注射方式,具有非侵入性、簡單易行的特點,更為重要的是它能夠直接通過嗅覺神經通路進入大腦,繞過血腦屏障,直接遞送到中樞神經系統。
這不僅提高了外泌體的生物利用率,還避免了其在胃腸道和肝臟中的代謝損失。此外,鼻腔施用還具有起效快、副作用小等優點
我們也是期待現有的研究可以早日開花結果,為眾多有需求的人帶來新的應對策略。
【注】文章內容旨在科普細胞知識,進行學術交流分享,了解行業前沿發展動態,不構成任何應用建議。

