發布時間:2025-10-22 瀏覽量:0
前言
INTRODUCTION
國家衛健委發布的數據顯示,我國有超過2.5億人飽受脫發困擾,平均每6人就有1人加入“脫發大軍”。更值得關注的是,這一問題正逐漸低齡化,26-30歲尤其成為脫發高發年齡段,曾經多見于中年人的發際線后移,如今已成為不少“打工人”的常見困擾。

一般情況下,正常成人每日掉50-100根為生理性脫發。若每日脫發超100根且持續較久,或脫發量未超100根但明顯增多,伴隨頭發變稀、禿斑、發際線后移等,可能是病理性脫發,需及時就醫。
常見脫發類型中,雄激素性脫發(androgenetic alopecia;AGA)最常見,與遺傳、激素水平等多種因素有關,男性多表現為前額與頭頂頭發稀疏,女性則以頭頂部頭發變薄為主要特征,其核心病理機制為毛囊微型化,隨著年齡的增加,AGA的發生率顯著上升。
雖然現有針對AGA的治療方法有很多,但大多存在一定的局限性:
· 米諾地爾外用用藥繁瑣,可能引發頭皮刺激或毛囊炎;
· 非那雄胺口服治療周期長,副作用難以接受而導致依從性差,且對女性完全禁用;
· PRP血漿療法恢復期較長,且效果持續性不強;
· 植發手術費用高昂,術后恢復期較長且依賴供體毛囊資源。
外泌體是直徑30-150 納米的囊泡,由細胞分泌并攜帶蛋白質、核酸、脂質等生物活性分子。它們像“微型快遞包裹”,將修護信號傳遞給靶細胞,激活通路,這些特性都使得干細胞外泌體應對雄激素性脫發成為可能。外泌體應對脫發的作用機制主要在于:
激活毛囊細胞
激活毛囊干細胞:通過調節Wnt/β-catenin信號通路、BMP家族及生長因子(如VEGF、IGF-1),喚醒休眠毛囊干細胞,延長生長期,逆轉毛囊微型化;
促進血管新生
外泌體中的VEGF等因子刺激頭皮血管生成,改善毛囊營養供給;
關于修護微環境
應對毛囊細胞的炎癥反應,提高毛囊細胞的生存率和再生能力,應對雄激素性脫發誘導的炎癥反應,減少毛囊周圍免疫細胞浸潤,保護毛囊免受損傷。
臨床試驗1:
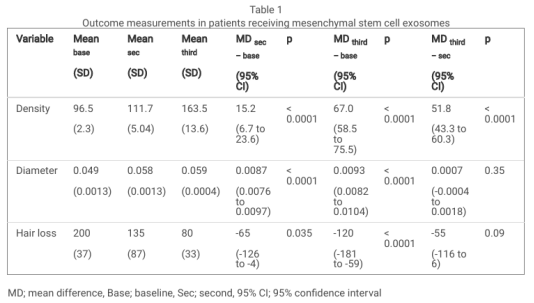
12名雄激素性脫發患者(男性7名,女性5名),年齡18-60歲,脫發等級為男性Norwood III-IV級或女性Ludwig I-II級。接受胎盤干細胞外泌體的臨床研究,每14天一次,最多4次。
結果發現:基線時平均頭發密度為96.5根/cm2,頭發直徑0.049 mm,脫發數量200根。干預后,平均頭發密度在6周時增加了69.4%;頭發直徑在3周和6周時分別增加至0.058 mm和0.059 mm;平均脫發數量在6周時顯著減少至80根,未觀察到顯著不良反應或臨床實驗室指標變化。
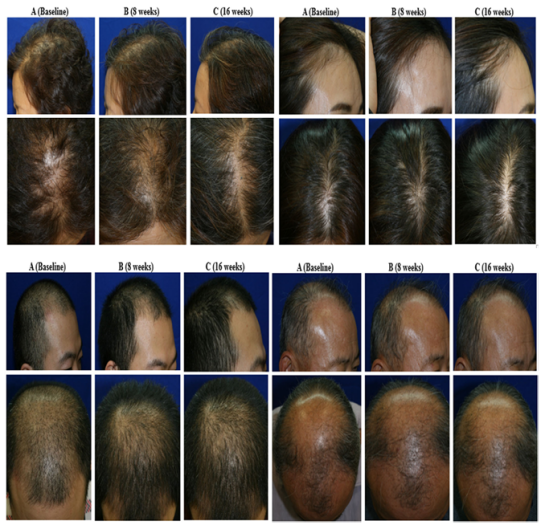
臨床試驗2:
一項雄激素性脫發外泌體治療的研究納入了38位年齡在18至59歲之間的受試者,接受脂肪干細胞外泌體治療。經過16周的臨床研究后,實驗組在頭發數量上實現了19.2%的增長,頭發密度相對于基線的總體百分比變化為28.1%。此外,實驗組在毛發直徑上也有顯著改善,總百分比變化達到了14.2%。
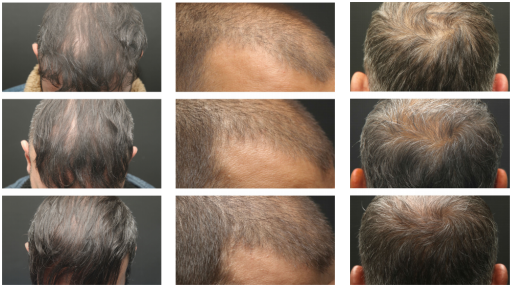
臨床試驗3:
在30名22-65歲的III–VI級男性脫發患者頭皮的3個區域應用干細胞外泌體進行臨床研究。結果發現:平均頭發密度明顯增加,參與研究前的149.7根 /cm2 在參與臨床研究后第4周增加到153.6根 /cm2,并在第12周進一步增加到157根 /cm2,且受試者對效果的滿意度在12周時較4周時明顯提高。
脫發不僅是美學問題,更影響心理健康與生活質量。外泌體多靶點、精準化的干預方式,較傳統雄激素性脫發治療方法更具針對性,為實現更高效的治療效果奠定了基礎。此外,外泌體有望與現有藥物治療、植發手術等手段協同作用,形成優勢互補。隨著技術的不斷進步,外泌體的提取純化工藝將逐步完善,更多的臨床研究將深入探索外泌體技術長期效果和適用人群,有望為廣大有需求的朋友帶來更安全、高效、持久的新選擇,推動脫發治療進入新的階段。
【注】文章內容旨在科普細胞知識,進行學術交流分享,了解行業前沿發展動態,不構成任何應用建議。

